钟文昭医生的科普号
- 精选 广东省肺癌研究所荣获全国卫生计生系统先进集体称号
2017年8月17日下午,全国卫生计生系统表彰大会在京召开,对全国卫生计生系统先进集体、先进工作者和劳动模范及“白求恩奖章”获得者进行表彰。此次广东省荣获表彰:“白求恩奖章”1名、先进集体12个和先进工作者51名。省卫生计生委主任段宇飞及人事处负责人带队参加全国表彰大会。广东省肺癌研究所荣获“全国卫生计生系统先进集体”称号,受到国务院副总理刘延东和国家卫生计生委主任李斌等国家和部委领导的亲自接见和表彰图:广东省肺癌研究所或全国卫生计生系统先进集体中共中央政治局委员、国务院副总理刘延东出在本次会议上做出重要讲话,传达了习近平总书记关于“党和国家始终高度重视发展卫生和健康事业、增进人民健康福祉”的重要指示和李克强总理关于“推进卫生计生事业改革发展,关系人民群众身心健康,关系全面建成小康社会”的批示。同时,刘副总理充分肯定了广大医务人员为建设健康中国作出的卓越贡献,号召全社会尊重生命,尊重医护工作者的辛勤劳动,营造和谐医患关系。卫生计生系统干部职工要紧密团结在以习近平同志为核心的党中央周围,深入贯彻习近平总书记重要指示精神,不忘初心,不负重托,敬业奉献,守护健康,努力打造成符合健康中国需要、人民群众满意的高素质卫生计生队伍,为推进卫生健康事业实现新跨越,全面建成小康社会作出新贡献。图:荣获本次表彰的广东省各单位代表在广东省卫生计生委召开的获奖代表座谈会上,段宇飞主任指出,获得表彰的集体和个人是我省82万医务工作者的优秀代表,是我省卫生计生系统的骄傲,他们用实际行动彰显了大医精诚、医者仁心的医学传统,诠释了“敬佑生命、救死扶伤、甘于奉献、大爱无疆”的职业精神,为保障全省人民群众健康安全,推进健康广东建设做出了积极的贡献。十载磨砺,风雨兼程广东省肺癌研究所在广东省省委、省政府、省卫生厅的大力支持下于2003年1月成立,由在肺癌领域享有国际声誉的著名专家吴一龙教授作为创始人。2008年5月广东省编办发文正式成立“广东省肺癌研究所”。现由肺一科、肺二科(肺外科)、肺三科、胸外科、肺四科(胸部肿瘤科)、放射治疗科、肿瘤介入科,生物统计室、信息中心、广东省肺癌转化医学重点实验室(包括生物材料库和华南临床基因检测中心)、《循证医学》杂志社及临床药理基地等多个临床与科研科室组成。肺研所立足多学科单病种管理的肺癌精准诊疗模式:汇集胸外科、肺内科、放射治疗、介入治疗、分子诊断等多学科诊疗优势,对肺癌患者进行全面分析权衡,为肺癌患者提供更优质的诊疗服务。目前设置床位522张,年住院量8100多人次,年手术2000余台次。在岗医务人员和研究人员共120余人,各科带头人及业务骨干大部分为留学(研修)归国人员。肺研所与美国、英国、丹麦、德国、日本、澳大利亚、韩国等国家的肿瘤防治机构有广泛的交流与合作,各项医疗服务力求与世界同步。研究所学科设置相对齐全、技术力量雄厚、仪器设备先进。研究所利用多种高端医学技术平台为患者服务,包括正电子发射断层扫描(PET/CT)、高分辨率CT、高能量直线加速器、调强适形放疗、数字减影血管造影、全自动血液生化分析仪、核磁共振仪等先进的仪器设备,集肿瘤医疗、科研、教学为一体,拥有广东省科技厅立项支持建设的“广东省肺癌转化医学重点实验室”(前身为中心实验室),开展国际先进的靶向分子诊断和研究,集肿瘤科学研究和临床分子预测功能于一身励精图治,敢为天下先自2003年创立,弹指一挥间,广东省肺癌研究所已经14周岁了。14年来,在吴一龙教授的带领下,广东省肺癌研究所走出了一条独特的发展之路,集肺癌多学科综合治疗为一体,将临床试验和转化医学融合成体系,是研究所的力量之源;国际化视野的高起点,转化应用的布局,合作共赢的胸襟,是研究所成功的基石。创立中国胸部肿瘤协作组(CTONG),促进胸部肿瘤医疗、科研活动规范化、现代化和国际化,创立多中心合作的良好共赢模式,提高我国胸部肿瘤诊治水平和国际地位、为临床实践提供高级别循证医学证据。直到今天,在NEJM、lancet、lancet oncol、Nature genetic、JCO、Cancer cell等全球高影响因子的肿瘤学顶尖期刊上,已多次留下广东省肺癌研究所和CTONG成员单位的名字。通过积极参与药物研发的国际化协作,领衔国际临床试验开展,并且积极倡导和探索原创性研究,由跟随到参与,由参与、弄潮到领潮。召开十四届中国肺癌高峰论坛,每次针对一个肺癌临床实践中备受关注,争议最大的论题进行纵深探讨,集合内、外、放疗、病理、影像、基础研究甚至政策层面的专家形成国内共识,指导临床。图:中国胸部肿瘤研究协作组(CTONG)创立初期成员合照吴一龙教授精于肺癌“精准医学”诊治及研究数十年,创立的“肺癌分子靶向精准治疗模式”和“肺癌系统性纵隔淋巴结清扫术”已纳入我国《原发性肺癌诊疗规范》和《中国肺癌临床指南》以及英国、美国、德国、日本、欧洲等国家和地区制订的肺癌指南。吴教授被授予美国外科学院院士荣誉称号、国际肺癌研究协会(IASLC)理事会理事、IASLC国际肺癌分期委员会委员中来自中国唯一的一位专家委员,担任中国临床肿瘤学会(CSCO)理事长。吴一龙教授荣获2015年国际肺癌研究协会(IASLC)颁发的Paul Bunn Jr. Scientific Award (杰出科学奖),成为世界肺癌研究学首位荣膺此奖的中国肿瘤临床科学家。此外,吴一龙教授还荣获了2015第十六届吴阶平-保罗杨森医学药学奖(简称“吴杨奖”),并荣获全国五一劳动奖章等荣誉。研究成果获得2016年中华医学会中华医学科技奖一等奖和2017年国家科技进步奖二等奖:通过对肺癌中EGFR等基因的分子分型和大样本系列试验研究,建立了EGFR精准靶向治疗新策略;进一步的“相嵌序贯”和亚型选择,将肺癌患者的生存时间进一步延长;结合临床耐药模式施以精准治疗,患者生存时间进一步优化延长至39个月,使EGFR突变型晚期肺癌逐渐成为临床可控的慢性病。作为CSCO理事长,吴教授近年来不断引领和推动具有中国特色的CSCO肺癌诊疗指南的制定和发布,基于肿瘤治疗价值,地域差异和药物可及性,为我国肺癌循证诊治的规范化模式建立发展奠定了基础。图:吴一龙教授获国际肺癌研究会(IASLC)的最高奖—Paul A. Bunn, Jr. Scientific Award(杰出科学奖)继往开来,成绩斐然十四年来,广东省肺癌研究所成长起一批中青年专业人才,团队骨干张绪超、杨衿记、周清、杨学宁、钟文昭、涂海燕、潘燚、贲晓松、陈华军、甘彬等也分别担任CSCO常委、执委会委员及副秘书长、CTONG 秘书长、广东省青年五四奖章、CSCO肿瘤生物标志物专家委员会秘书长、广东省抗癌协会肺癌专业委员会主任委员、广东省循证医学专业委员会主任委员、广东省女医师协会肺癌专业委员会主席、CSCO青委会副主任委员、《Journal of Thoracic Oncology》杂志副主编等重要学术组织任职。不仅如此,他们还是活跃在全球肺癌领域的中流砥柱,连续10年站在WCLC、ASCO、ESMO、AACR、CSCO等肺癌主要国际会议的讲台上,激扬文字,争鸣学术,阐述观点,发出中国肺癌诊疗研究团队的强音。图:肺研所团队骨干中心实验室由现任肺研所所长张绪超、标本库主任苏健、陈志红等带领,以多种分子分型技术、生物芯片、生物材料库建设等主要技术手段,侧重肺癌的分子预警、预测、预防的临床应用研究。为了更好的为患者提供先进的肺癌基因分型技术服务,实验室不断研发并建立了肺癌分子靶向治疗的预测标志物分析技术,包括EGFR突变、ALK融合、ROS1融合、MET变异、KRAS突变检测方法,用于预测靶向药物吉非替尼(Gefitinib)或厄洛替尼(Erlotinib)、克唑替尼(Crizotinib)、奥希替尼(Osimertinib)的疗效。此外,实验室还建立了基于qPCR、FISH、IHC、MassArray、NGS等技术的多基因检测技术,这些靶向药物耐药分子标记的检测将为临床患者的药物使用提供更精准的预测方法。 肺癌内科治疗团队坚持“个体化分子靶向治疗发展模式”:即根据患者具体情况,应用独特的个体化治疗评价体系,制定个体化的多学科综合治疗方案。针对每位肺癌患者,根据其肿瘤的分子分型特征,个体行为状态、个人意愿等建立“个体化”的治疗方案。对每个病人量体裁衣,设计出具有国际水平又针对个体特点的靶向精准诊治方案,让每一个病人在中心得到最佳且先进的医疗照顾。创立了“突变丰度”、“混合疗效”、“靶向治疗三种耐药模式”等指导临床实践的概念。近年来,肺研所外科团队成果迭出:杨学宁主任在肺外科管理中规范术前检查及手术流程,优化围术期康复治疗,开展高难度的ECMO下3-D胸腔镜气管肿瘤摘除、隆突成型、改良微创手术操作器械以及放疗科合作肺上沟瘤术中放疗。2016年7月,在“第三届中国胸外科菁英手术技艺大赛暨直通欧洲选拔赛”全国总决赛上,钟文昭作为南中国区腔镜肺切组第1名,登上全国决赛舞台并最终夺冠。2015年肺研所团队参加CSCO中日韩肺癌个体化诊疗大赛中国区冠军和中日韩总决赛冠军。目前科内包括聂强、廖日强、董嵩、江本元等6位主治以上医师在和心血管外科联合开展高难度手术、EBUS、磁导航支气管内镜诊断、术中流程化管理、肺部小结节精准定位、肺部结节人工智能诊断等方面各有建树。肺研所团队作为主要研究者,牵头多项围术期治疗多中心随机对照临床研究,如CSCL0201、CSCL0501、CTONG1103、CTONG1104已经或即将公布最终10年以上随访结果。值得一提的是,就在2017年6月,吴一龙教授在ASCO年会最大的报告厅就淋巴结转移患者术后治疗研究ADJUVANT临床研究做了肺癌专场的开场口头报告,改变肺癌外科术后治疗临床实践。放疗科以“精确放疗技术”为发展方向,开展体部立体定向放疗,已运用于肺癌、直肠癌、前列腺癌中;以国际AAPM协会规范为标准加强质量管理及质量控制,确保放疗整体治疗水平及治疗精度。在省内率先开展可移动式低能X线术中放疗技术,探索IORT在可手术肿瘤治疗中的价值。在临床已经运用于早期乳腺癌、肺上沟瘤的治疗。值得一提的是,肺尖癌术中放疗研究结果在德国曼海姆术中放疗会议上进行口头汇报并获会议最佳摘要奖,并在曼谷亚太术中放疗会议中作为大会主题发言。图:肺研所大家庭经过多年的发展,肺研所已经形成临床研究与转化性研究并重的学术体系:以临床研究为导向,促进本所临床用药和诊疗技术的先进性。设备先进的实验室为基础研究向临床实践的转化提供了良好的技术平台基础,不断将先进的分子遗传学测试转化应用于临床药物选择,提高了肺癌治疗疗效。未来,肺研所还将致力于提供诊治及预防预测全方位的临床服务:工作重点不仅限于“治已病”,还要“治未病”。为肿瘤患者提供筛查、防癌体检等早发现、早诊断、早治疗、早康复的优质服务。目标是能够形成肺癌预防、治疗、康复、患癌或癌症复发风险评估相结合的“一站式”服务机构。本次获奖是肺癌研究所团队精益求精的展示,更体现了其在肺癌全程管理和多学科治疗领域的厚积薄发,期待这支诊疗和科研为一体,内外放疗科并举的肺癌精锐团队的成果,能更好回答肺癌诊疗的问题,推动肺癌治疗理念进步,解除病患的痛苦。
钟文昭 主任医师 广东省人民医院 肺外科3447人已读 - 新辅助免疫化疗vs辅助免疫治疗
今天听大咖TetsuyaMitsudomi教授讲肺癌围术期免疫治疗进展,有两个比较大的体会:1,新辅助➕手术还是手术➕辅助好,看数据,会有一些患者经过新辅助免疫化疗后,由于治疗的副作用及身体条件,会失去手术机会,这个比例可能在15%左右,但其实我们看到IMpower010,从手术后随机到接受辅助免疫治疗,同样会有相当比例的患者,没办法真正的接受辅助免疫,所以之前的论调并不能完全站住脚。2,黑色素中已经有前瞻性随机对照研究,证实新辅助免疫治疗会比辅助免疫治疗更好,这可能与肿瘤本身充当原位疫苗以及区域淋巴结中免疫细胞趋势所发挥作用。
 张嘉涛 医师 广东省人民医院 肺外科22人已读
张嘉涛 医师 广东省人民医院 肺外科22人已读 - 右下肺静脉旁结节流域楔形切除
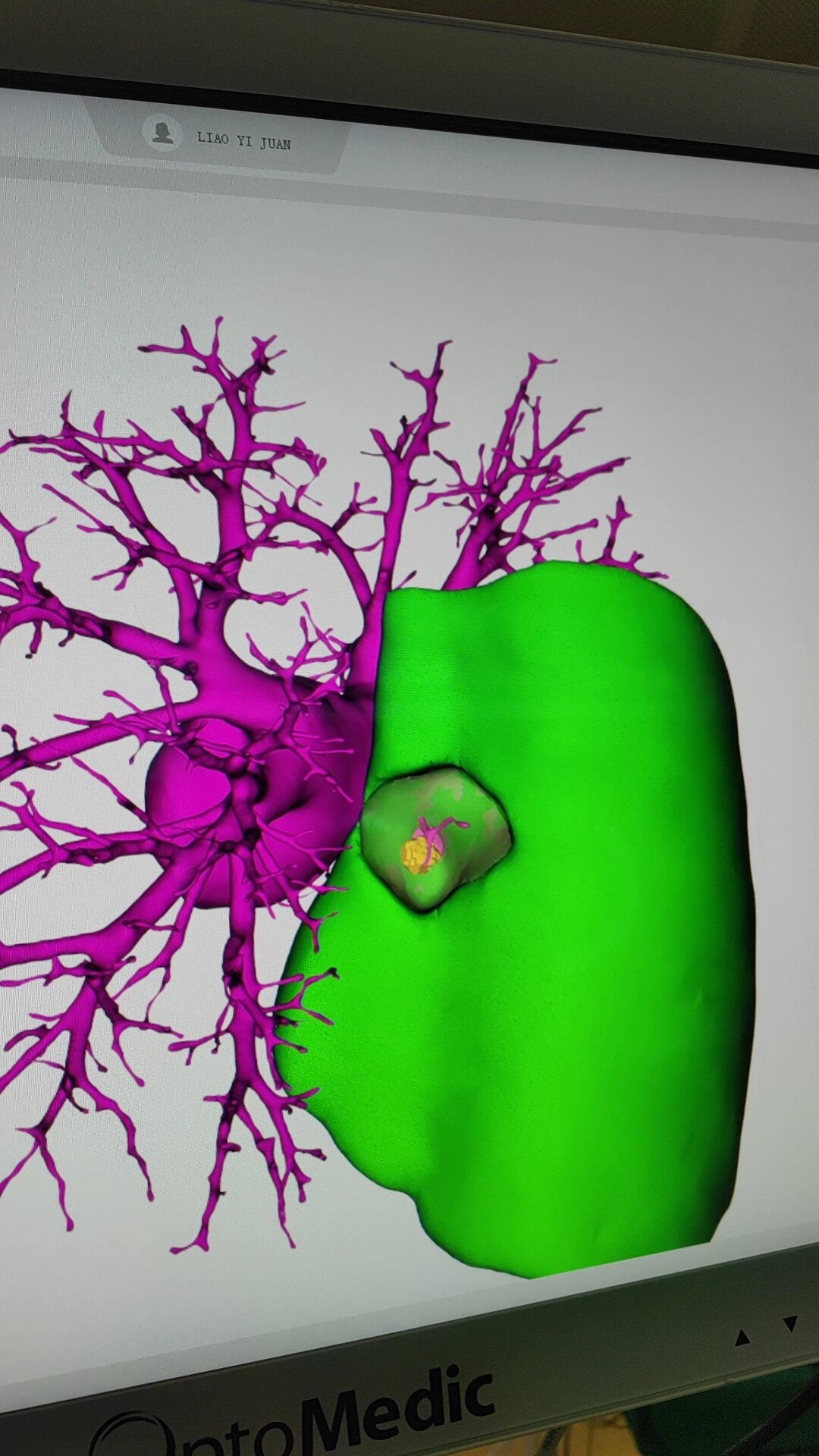
今天完成了一例比较独特的流域楔形切除!患者是一名40多岁女性,发现右下肺静脉旁一个混合密度结节,9mm左右,密度偏高,决定手术切除。这个患者的手术方案肺叶切除觉得还是可惜,于是尝试了流域楔形切除。根据三维重建,结节上下方刚好有一条很小的静脉分支,于是分别仔细地游离出来,离断后,通过ICG荧光就发现了流域地形图,尽量充分游离后楔形切除,冰冻提示腺癌,切缘阴性,区域淋巴结也是阴性。
 张嘉涛 医师 广东省人民医院 肺外科69人已读
张嘉涛 医师 广东省人民医院 肺外科69人已读 - 图文文章 第19期中国胸部肿瘤大会诊~湖北恩施
第19期中国胸部肿瘤大会诊,来到湖北恩施讨论了两个高难度病例:1,EGFR突变多线治疗后,经历了奥希替尼,赛沃替尼,局部放疗,全脑放疗这个病例从c-MET过表达病理判定标本,临床上什么时候用EGFR和MET抑制剂联合,什么时候单用,再到最后面是否重新靶向治疗再挑战,讨论过程确实精彩。2,双肺多发结节手术后,外周血MRD阳性处理这是一个很有特点的病例,从手术指证到治疗决策都挺有争议,指南上是没有标准治疗,这时候应该如何决策,从MRD阳性进行性升高应该如何指导下一步治疗?
 张嘉涛 医师 广东省人民医院 肺外科42人已读
张嘉涛 医师 广东省人民医院 肺外科42人已读 - 晚期ALK靶向治疗,肿瘤全消失!
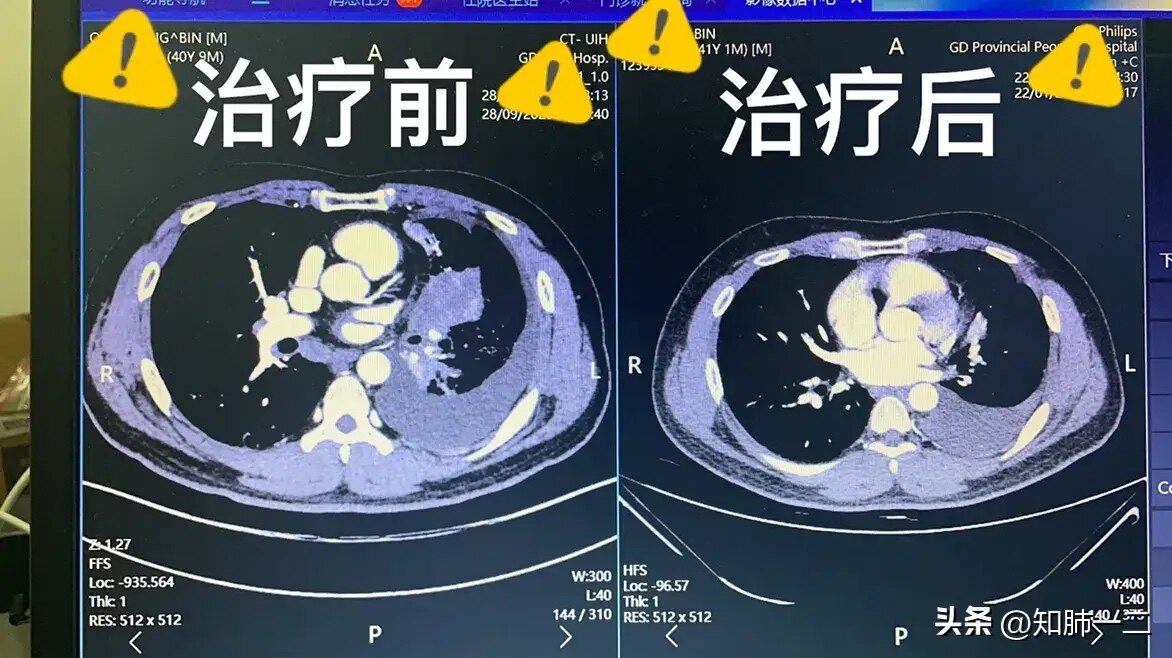
这是一个晚期ALK患者,当时双肺转移,伴有胸腔积液,经过靶向治疗后,双肺转移瘤消失,剩余左上肺残留病灶,进一步手术切除,神奇的疗效:术中看到胸腔积液还是有的,淡黄色清亮,细胞学提示未找到可疑癌细胞,术后大病理提示达到完全病理缓解,也就是切开来的肿物以及淋巴结都没找到活性肿瘤细胞!#广东省肺癌研究所##ALK#
 张嘉涛 医师 广东省人民医院 肺外科42人已读
张嘉涛 医师 广东省人民医院 肺外科42人已读 - 国际肺癌日科普直播
11月17日下午3点-4点半直播,欢迎扫描二维码观看,预留半小时线上提问解答!
 张嘉涛 医师 广东省人民医院 肺外科34人已读
张嘉涛 医师 广东省人民医院 肺外科34人已读 - 局部晚期肺癌MRD检测与早期的区别
局部晚期肺癌MRD检测研究荣登<CancerCell>,那么他到底与早期肺癌术后有什么不同?
 张嘉涛 医师 广东省人民医院 肺外科79人已读
张嘉涛 医师 广东省人民医院 肺外科79人已读 - 医学科普 《CSCO原发性肺癌诊疗指南2016.V1》钟文昭 主任医师 广东省人民医院 肺外科1597人已读
- 医学科普 从系统性到个体化淋巴结清扫的演变
近期何建行团队梁文华博士等在Journal of Clinical Onocoly上发表的题为“The Impact of Examined Lymph Node Count on Precise Staging andLong-term Survival of Resected NSCLC: A Population Study of the U.S.SEER Database and a Chinese Multi-Institutional Registry”的文章,通过中美数据趋势视角,提出16个量化的淋巴结清扫标准,引起广泛关注。吴一龙教授团队受邀对该研究撰写了JCO述评,并就该研究对临床实践启示,争议以及后续深入方向进行了探讨。
钟文昭 主任医师 广东省人民医院 肺外科1747人已读 - 医学科普 备战2017年,第八版TNM分期干货来了—看这一篇就够了
第八版的TNM分期就要开始使用,你是否已经准备好了?内容繁多的文献,各式各样的解读,是否已经眼花缭乱?为了让大家更好的理解跟快速掌握第八版TNM分期的更新要点,小编拉了研究免疫治疗的小编2号专门一起复习了2016 WCLC关于TNM分期的内容跟IASLC关于第八版分期的文献,希望提供最新最准确的内容,让大家能在最短时间学习并及时在2017年使用这个分期。大家可以收藏,随时重新打开学习,也可以转发给需要的同事或者同学哦,另外转发朋友圈也是极好的。TNM分期基于解剖学,是对肿瘤累及范围的精确描述。它与肿瘤的预后及治疗决策直接相关,是肿瘤患者诊治过称中至关重要的一个步骤。2015-2016年,IASLC相继推出TNM分期的建议,共计12篇文献1-12,对原有第七版分期做出了大量改变及补充,并将在2017.1.1开始正式使用,将对临床诊疗产生巨大影响。为了促进临床实践中第八版TNM分期的应用,本次在维也纳召开的第17届世界肺癌大会专门组织专家针对这一问题进行讲解及解疑,包括全体大会的Hisao Asamura13、RamónRami-Porta14等人。第八版TNM分期概述肺癌TNM分期系统的制定是一个复杂的过程,除了需要不同专科医师(外科医师、内科医师、放疗科医师、病理科医师等)参与、还需要不同机构(IASCL、UICC、AJCC)的不断讨论确定。制定TNM分期系统过程中,纳入的病例需要遵循以下基本原则:第一、所有的病例均经过显微镜下病理确认为恶性肿瘤,包括组织类型;第二、每个病例要求有两个分期:1.临床分期:cTNM,其中经纵隔镜组织学确认的N2淋巴结转移,也定义为临床分期(cN2);2.病理分期:pTNM,仅用于手术切除标本;第三、确定T、N、M和/或pT、pN、pM分类和总分期后,不得在病历上进行再次修改;第四、当某一病例的T/N/M分类存在疑问时,应选择较低(分期较早)的分期。要点一:T、N、M各分期的更新本次关于TNM分期的改变主要为T分期,N分期无改变,M分期有少量改动。T分期10的改变内容主要包括:1.T≤5cm时,每1cm作为一个亚组(T1a、T1b、T1c、T2a、T2b);5cm<T≤7cm归为T3;T>7cm归为T4;2.原T3更改,包括:a.部分降为T2(肿瘤距离隆突<2cm、全肺不张);b.部分升为T4(肿瘤侵犯膈肌);c.弃用部分T3分类(纵隔胸膜侵犯);1.脏层胸膜侵犯适用于病理分期,根据是否累及弹性纤维层判定;2.T分期中加入Tis,并进一步细分为Tis(AIS),即原位腺癌,和Tis(SCIS)原位鳞癌;加入T1mi,即微浸润腺癌。病理亚型更加广泛加入到T分期中。第八版分期对N分期1无调整,因第七版N分期对于生存的预测效果良好,但是建议临床医师在临床工作中,可对淋巴结进一步分类(Table 1),为未来的新分期做准备:M分期7的改变在于将单个器官单个病灶转移从胸腔外转移病例中分离出来,并定义为M1b,而多个器官转移或者单个器官多个转移则更改为M1c,M1a则无改动。M1a:胸腔内播散/转移,包括双肺/胸膜/心包结节、恶性胸腔/心包积液;M1b:胸腔外单个器官单个病灶转移;M1c:胸腔外多个器官或单个器官多个病灶转移。总分期的改变主要改变由T分期及M分期引起,变化如下(见Figure1):1. T1a、T1b和T1c(N0M0)分别归为IA1、IA2和IA3期;2.针对T1a-T2a(N1M0),由IIA期归为IIB期;3.针对T3N2M0,由IIIA期归为IIIB期;4.针对T3/T4(N3M0),由IIIB期归为IIIC期;5.针对M分期,将M1a和M1b归为IVA期,M1c归为IVB期。Figure 1 TNM grouping(Adjusted fromRamón Rami-Porta’s presentation14)另外,小编根据TNM分期里面提供的数据表格,整理了一下各T分期的淋巴结转移率(Table 2),能让大家对这个有一个大体的印象。另外,针对各分期的前缀(临床分期、病理分期等),定义可见table 3。要点二:新增磨玻璃结节(GGO)的测量及T分期对于近年来受到外科关注的GGO和混杂GGO结节,在新分期12中根据实性成分大小决定T分期。对于GGO病例,实性成分对预后具有重要的影响,且影像学上的实性成分往往预示其浸润性,因此,临床分期时要求测量CT图像实性成分大小(1mm层厚,肺窗)、病理分期要求使用浸润性成分大小作为T分期的依据(Figure 2)。关于这部分,小编原来专门写过一篇文章。原文链接 http://mp.weixin.qq.com/s/89crGdoe-xFB_MJv7Sw4vQ要点三:肺部多发病灶的诊断及分期肺部多发病灶的TNM分期6由病灶的临床表现、病理学关联和生物学行为共同决定。根据这一标准,共有4种疾病模式(Figure3):1.对于第二原发肺恶性肿瘤,每一个肿瘤单独进行T、N、M分期;2.对于肺内转移病灶,不同病灶的组织学类型相同时(无论是怀疑还是已经证实),应根据肿瘤的位置决定其分期,如T3(病灶位于同一叶)、T4(病灶位于同侧不同肺叶)、M1a(另有病灶位于对侧肺);3.对于肺部多发GGO或者病理证实为贴壁样生长型肿瘤,T分期由T分期最高的结节决定,后面括号内加上结节数目或者m,如T1a(3)N0M0,括号内的数字不包含小于5mm的纯GGO结节/AAH/可疑良性病变,注:几乎完全为实性或者浸润性的肿瘤(GGO或贴壁样成分<10%)不适用这个方法,应单独进行分期;4.对于弥漫性肺炎型腺癌(diffusepneumonic-type adenocarcinoma),肿瘤位于单一肺叶时定义为T3,累及同侧另一肺叶时定义为T4,累及对侧肺时定义为M1a。这类肿瘤往往是浸润性黏液腺癌,转移少见。这个方法同样适用于肺部多发粟粒样病变。上述后三种情况均仅有一个N分期及M分期。Figure3. Representative examples of four patterns of disease with multiple pulmonarysites在存在肺部多发结节的病例,建议多学科团队综合影像学及病理学特征来区分转移及多原发肿瘤,当病理类型不同或者切除标本的详细病理学评估显示特征不同时,考虑为多原发肿瘤,当比较基因组学提示序列相同时,则考虑转移结节。另外,还有其他辅助判断的临床病理特征,供临床分期及病理分期使用(Table 4, Table 5, Figure4)。第八版TNM分期相对第七版,有着其创新之处,让肺癌工作中更好的根据分期划分各组的预后,有利于未来的临床试验对肿瘤病人进行分层,提高各期病人的同质性。TNM分期的制定基于大样本数据,对临床指导价值巨大,但是在临床应用会存在诸多问题,可能导致应用不准确,因此本次大会专门为TNM分期进行解释。但是TNM分期仍存在不少问题:1.病例数据来源不平衡,绝大部分病例由欧洲(46560,49%)及亚洲(41705例,44%)提供,总体病例分布在各大洲之间并不平衡;2. N的分期相对复杂,除日本使用Naruke标准,全球其他地方均使用ATS标准;3.不同外科医师和病理科医师对标本的处理可能存在差异,导致N2分期难度增大。因此未来对于TNM分期的制定还有赖于全球各地区的努力,使其更具代表性及更加规范化。目前已经开始第九版TNM分期的工作,预计在2024年发表。下一版分期仍然按照预后对TNM分期进行调整,而目前分子标志物对患者的预后影响大,关于是否将其纳入TNM分期存在争议,来自日本的Hisao Asamura教授强调:TNM分期是一个基于解剖学的分期系统,因此可能不会将其纳入分期系统中,下一版的TNM分期仍然会着重于预后来分析。关于TNM的进一步发展,重点可能还在于GGO和IIIA N2病例,其具有一定的复杂性和治疗决策的差异性,希望后续发展能为这部分病人的诊疗提供依据,使得这部分病人能得到更加个性化、精准化的治疗。而TNM分期对亚肺叶切除的指导意义,不仅取决于病灶大小,还与病灶的CT表现类型、肿瘤生长速度、肿瘤代谢情况、病理类型及亚型、淋巴结是否转移有关,希望正在进行的三个亚肺叶切除的临床试验(JCOG0802/WJOG4607L16,CALGB 14050317,STEPS(NCT02360761)18)能给出部分答案,未来的TNM分期可能在这方面会有一定的体现。Reference:1. Asamura H, Chansky K, Crowley J, et al. TheInternational Association for the Study of Lung Cancer Lung Cancer StagingProject: Proposals for the Revision of the N Descriptors in the Forthcoming 8thEdition of the TNM Classification for Lung Cancer.Journal of thoracic oncology : official publication of theInternational Association for the Study of Lung Cancer2015;10(12): 1675-84.2. Detterbeck FC, Bolejack V, Arenberg DA, et al. The IASLC LungCancer Staging Project: Background Data and Proposals for the Classification ofLung Cancer with Separate Tumor Nodules in the Forthcoming Eighth Edition ofthe TNM Classification for Lung Cancer.Journalof thoracic oncology : official publication of the International Associationfor the Study of Lung Cancer2016;11(5):681-92.3. Detterbeck FC, Chansky K, Groome P, et al. The IASLC Lung CancerStaging Project: Methodology and Validation Used in the Development ofProposals for Revision of the Stage Classification of NSCLC in the Forthcoming(Eighth) Edition of the TNM Classification of Lung Cancer.Journal of Thoracic Oncology2016;11(9): 1433-46.4. Detterbeck FC, Franklin WA, Nicholson AG, et al. The IASLC LungCancer Staging Project: Background Data and Proposed Criteria to DistinguishSeparate Primary Lung Cancers from Metastatic Foci in Patients with Two LungTumors in the Forthcoming Eighth Edition of the TNM Classification for Lung Cancer.Journal of thoracic oncology : officialpublication of the International Association for the Study of Lung Cancer2016;11(5): 651-65.5. Detterbeck FC, Marom EM, Arenberg DA, et al. The IASLC Lung CancerStaging Project: Background Data and Proposals for the Application of TNMStaging Rules to Lung Cancer Presenting as Multiple Nodules with Ground Glassor Lepidic Features or a Pneumonic Type of Involvement in the ForthcomingEighth Edition of the TNM Classification.Journalof thoracic oncology : official publication of the International Associationfor the Study of Lung Cancer2016;11(5):666-80.6. Detterbeck FC, Nicholson AG, Franklin WA, et al. The IASLC LungCancer Staging Project: Summary of Proposals for Revisions of theClassification of Lung Cancers with Multiple Pulmonary Sites of Involvement inthe Forthcoming Eighth Edition of the TNM Classification.Journal of thoracic oncology : official publication of theInternational Association for the Study of Lung Cancer2016;11(5): 639-50.7. Eberhardt WE, Mitchell A, Crowley J, et al. The IASLC Lung CancerStaging Project: Proposals for the Revision of the M Descriptors in theForthcoming Eighth Edition of the TNM Classification of Lung Cancer.Journal of thoracic oncology : officialpublication of the International Association for the Study of Lung Cancer2015;10(11): 1515-22.8. Goldstraw P, Chansky K, Crowley J, et al. The IASLC Lung CancerStaging Project: Proposals for Revision of the TNM Stage Groupings in theForthcoming (Eighth) Edition of the TNM Classification for Lung Cancer.Journal of thoracic oncology : officialpublication of the International Association for the Study of Lung Cancer2016;11(1): 39-51.9. Nicholson AG, Chansky K, Crowley J, et al. The InternationalAssociation for the Study of Lung Cancer Lung Cancer Staging Project: Proposalsfor the Revision of the Clinical and Pathologic Staging of Small Cell LungCancer in the Forthcoming Eighth Edition of the TNM Classification for LungCancer.Journal of thoracic oncology :official publication of the International Association for the Study of LungCancer2016;11(3): 300-11.10. Rami-Porta R, Bolejack V, Crowley J, et al. The IASLC Lung CancerStaging Project: Proposals for the Revisions of the T Descriptors in theForthcoming Eighth Edition of the TNM Classification for Lung Cancer.Journal of thoracic oncology : officialpublication of the International Association for the Study of Lung Cancer2015;10(7): 990-1003.11. Rami-Porta R, Bolejack V, Giroux DJ, et al. The IASLC lung cancerstaging project: the new database to inform the eighth edition of the TNMclassification of lung cancer.Journal ofthoracic oncology : official publication of the International Association forthe Study of Lung Cancer2014;9(11):1618-24.12. Travis WD, Asamura H, Bankier AA, et al. The IASLC Lung CancerStaging Project: Proposals for Coding T Categories for Subsolid Nodules andAssessment of Tumor Size in Part-Solid Tumors in the Forthcoming Eighth Editionof the TNM Classification of Lung Cancer.Journalof thoracic oncology : official publication of the International Associationfor the Study of Lung Cancer2016.13. Asamura H. What’s New in 8th Ed of TNM Classification for LungCancer. 2016 WCLC.14. Rami-Porta R. Lung Cancer Staging Changing the Clinical Practice.2016 WCLC.15. Detterbeck FC, Boffa DJ, Kim AW, Tanoue LT. The 8th Edition LungCancer Stage Classification. Chest. 2016 Oct 22. pii: S0012-3692(16)60780-8.doi: 10.1016/j.chest.2016.10.010.16. Nakamura K, Saji H, Nakajima R, et al. A phase III randomized trialof lobectomy versus limited resection for small-sized peripheral non-small celllung cancer (JCOG0802/WJOG4607L).Japanesejournal of clinical oncology2010;40(3):271-4.17. National Institutes of Health. National Cancer Institute.CALGB-140503. A Phase III Randomized Trial of Lobectomy Versus SublobarResection for Small (≤ 2 cm) Peripheral Non-Small CellLung Cancer.[Last accessed Dec 14, 2016].18. Jun Wang. Surgical Treatment of Elderly Patients With Early StageNon-small Cell Lung Cancer (STEPS): Comparison Between Sublobar Resection andLobectomy - an Open, Multicenter, Randomized Phase III Clinical Trial.Available at: https://clinicaltrials.gov/show/NCT02360761. [Last accessed Dec14, 2016]
钟文昭 主任医师 广东省人民医院 肺外科3201人已读





